
-
 专利
专利 -
 商标
商标 -
 版权
版权 -
 商业秘密
商业秘密 -
 反不正当竞争
反不正当竞争 -
 植物新品种
植物新品种 -
 地理标志
地理标志 -
 集成电路布图设计
集成电路布图设计 -
 技术合同
技术合同 -
 传统文化
传统文化
律师动态
更多 >>知产速递
更多 >>审判动态
更多 >>案例聚焦
更多 >>法官视点
更多 >>裁判文书
更多 >>“生物医药技术许可交易License-in/out中重视并做好尽职调查,至关重要。通过相对完备的知识产权尽职调查全面且深入的了解拟交易标的药品的相关技术实际情况,从中发现风险点以及关键问题,为交易方案的制定提供依据,保证技术交易安全以及降低交易风险。”
一、近年来中国生物医药技术许可交易概况
生物医药行业事关民生,也是知识产权保护与冲突的集中领域之一。伴随着中国生物医药市场的逐渐完善以及蓬勃发展,不管是 First-in-Class 的原研药,还是 Me-too、Me-better、 Fast-follow、Best-in-class的仿制药,生物医药行业已成为众多投资机构的高度关注领域,同时中国生物医药领域的技术许可交易License-in/out 在近十年也由起步进入了快速发展阶段。 基于相关公开信息报道【1】,笔者对 2013-2022年中国药企授权引进 (License in )以及对外授权(License out)项目进行了初步的统计 (请见如下图1、图2) 。其中2021年中国 License in、License out 的交易数量分别为 149 个和55 个,交易总量达到历史新高;2022年中国医药交易热度略有下降,License in交易量锐减,但2022年中国 License out交易量再创新高,总体来说,随着国内药物研发越来越受到全球医药界的关注,预计中国医药公司的对外许可交易将有所增加。
图1 2013-2022年中国药企授权引进项目数量
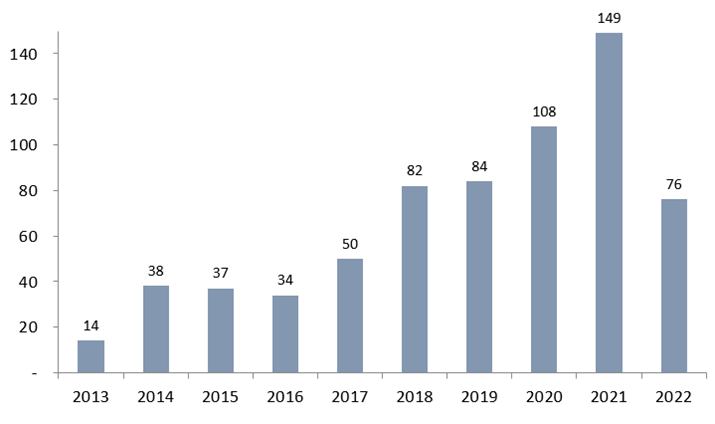
图2 2013-2022年中国药企对外授权项目数量
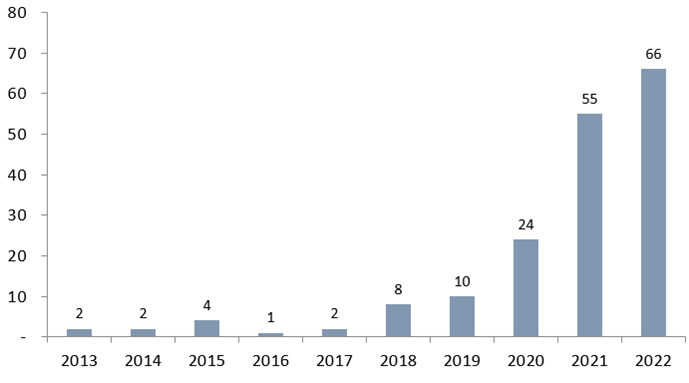
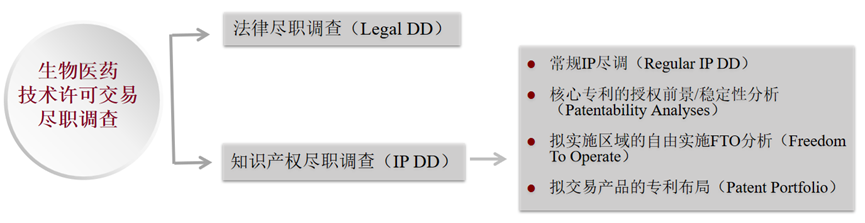
鉴于本身生物医药行业具有行业技术壁垒高、研发成本高、周期长、临床试验不确定、监管严格等特点,这也就导致了生物医药企业在进行授权许可交易时难免会面临诸多的不确定性以及风险。因此,在医药技术许可交易中重视并做好尽职调查,至关重要。一般而言,生物医药授权许可交易中的尽职调查一般由法律尽职调查(Legal Due Diligence,简称Legal DD)及知识产权尽职调查(Intellectual Property Due Diligence,简称IP DD)两部分组成。Legal DD一般由交易律师团队负责,IP DD则由知识产权律师团队负责完成,其中IP DD除了包括知识产权权属、法律状态、相关协议以及知识产权纠纷等常规IP尽调(Regular IP DD)外,考虑到生物医药领域涉及的技术专业性强、技术门槛高,出于交易安全的考虑,交易方同时会更加关注拟交易药物产品的核心专利授权前景/稳定性(Patentability Analyses)、拟实施区域是否可自由实施(Freedom To Operate)、拟交易产品的专利布局(Patent Portfolio)是否完备。如下图3给出了生物医药技术许可交易中尽职调查的内容列表。
图 3 生物医药技术许可交易尽职调查
本文将就生物医药技术许可交易中的知识产权尽职调查内容展开论述。出于篇幅考虑,笔者基于团队过往服务生物医药技术许可交易的经验,将主要针对拟交易产品的核心专利的授权前景/稳定性分析(Patentability Analyses)、拟实施区域的自由实施FTO分析(Freedom To Operate)、拟交易产品的专利布局(Patent Portfolio)展开分析,对于Regular IP DD部分本文在此将不再具体展开论述。同时需要说明知识产权尽职调查在医药企业研发(在研、预研)、药品商业化推广、投融资并购以及IPO上市过程中同样至关重要。
二、生物医药技术许可交易中的知识产权尽职调查介绍
(一)核心专利的授权前景/稳定性分析(Patentability Analyses)
专利申请并不等同于专利授权,即使专利授权也无法排除该等已授权专利存在被无效的可能性,再退一步,即使该等专利授权且稳定性较高,但获得的授权范围比较小,那么也无法涵盖拟交易药品的技术方案,达不到通过专利权保护药品的作用,尤其是拟交易的标的是原研创新药,只有获得专利才能建立竞争壁垒,一旦核心专利没有获得良好的授权保护范围,一定程度上无法规避仿制药厂。
如果拟交易的药品标的对应的核心专利尚未授权(处于pending 状态),那么则需要具有生物医药技术背景的专利律师对该等专利的授权前景进行分析,即该等专利是否授权可能性较大(提醒:此处的授权并非仅仅是指获得法律状态上的专利授权,而是需要分析是否相应核心专利可以获得涵盖拟交易产品技术方案的保护范围)。如果拟交易的药品标的对应的核心专利已授权,那么则需要对该等专利的稳定性进行分析,即该等专利是否存在被无效的可能性。如果经分析后认为,该等核心专利的授权前景并不明朗、或者专利后续授权的范围会比较小,或者虽已授权但被无效的可能性较大,可以建议客户调整拟交易项目的估值或结合技术交易项目的特点考虑在交易文件上如何设置相关条款以保护交易方利益。笔者所在团队曾参与处理的一项国内企业引进境外的小分子化药项目,拟引进药物的核心化合物结构专利尚未在中国获得授权,且根据中国专利局的审查意见,该化合物专利的授权前景并不明朗,基于授权前景分析,我们建议客户重点核查该技术引进项目若化合物结构在中国没有获得专利保护对客户作为被许可人(Licensee)的影响,并对后续可能采取的相应的专利分案、优先权新案策略提出建议,同时建议在交易文件中设置相应的条款以规制风险。
(1)授权前景分析
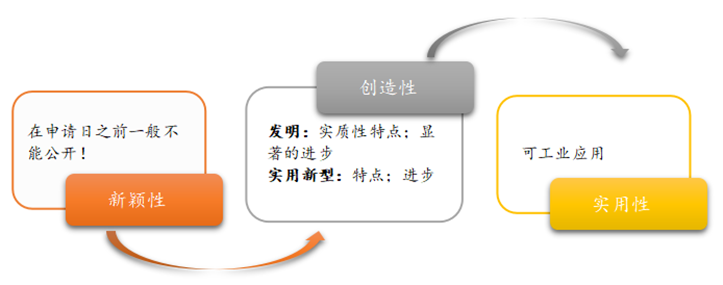
在进行核心专利授权前景分析时,根据中国专利法的规定,授予专利权的发明,应当具备新颖性、创造性和实用性【2】,即获得专利的条件,一般需要满足上述三性(请见如下图 4),一般专利不会涉及实用性问题,更多是涉及新颖性和创造性的问题。但同时也需要说明,生物医药技术壁垒较高,涉及生物医药的专利授权问题同时会涉及其他较为复杂的问题,比如是否存在公开不充分、得不到说明书支持、补充实验数据是否可被接受等问题,而这些均需要生物医药背景的知识产权律师结合具体的技术进行法律分析。
关于新颖性,以小分子化药专利举例说明,原则上,小分子化合物通式结构不能破坏该通式中一个具体化合物的新颖性,一个具体化合物结构的公开使包括该具体化合物的通式结构的权利要求丧失新颖性,但不影响该通式结构所包括的除该具体化合物以外的其他化合物的新颖性。关于创造性,在笔者处理的一项涉及小分子化合物投资交易中,笔者在进行对应的化合物通式核心专利授权前景分析中,就涉及到了生物电子等排体对化合物创造性的判断,我们认为在确定药学活性物质的创造性时,重要的并不是化合物的特定子结构是否被另一个已知的等排体替代,而是能否获知这样的具体化合物基团的替代对药学活性的影响,基于我们前期检索到的在先专利以及在先文献,在没有进一步信息的情况下,本领域技术人员没有任何理由合理预期将两个等排体替换得到的化合物会保持期望的活性,甚至取得了更好的活性,因此对于所属领域技术人员而言是非显而易见的,因而具备创造性。而在笔者处理的另一款小分子化药交易的授权前景分析中,就涉及到了补充试验数据是否能被采信的问题,根据我国《专利审查指南》第 3.5 节“关于补交的实验数据”的相关规定“对于申请日之后申请人为满足专利法第二十二条第三款、第二十六条第三款等要求补交的实验数据,审查员应当予以审查。补交实验数据所证明的技术效果应当是所属技术领域的技术人员能够从专利申请公开的内容中得到的”,而该等核心化合物的相关实验效果的数据并未在说明书中公开同时也未记载相关的技术效果,那么对于说明书中未记载的技术效果,无论补充提交的实验数据是否可以证明该效果在申请日前已得到实验验证,该技术效果在创造性评价中均不予考虑。
图4 获得专利的条件 - 三性
(2)稳定性分析
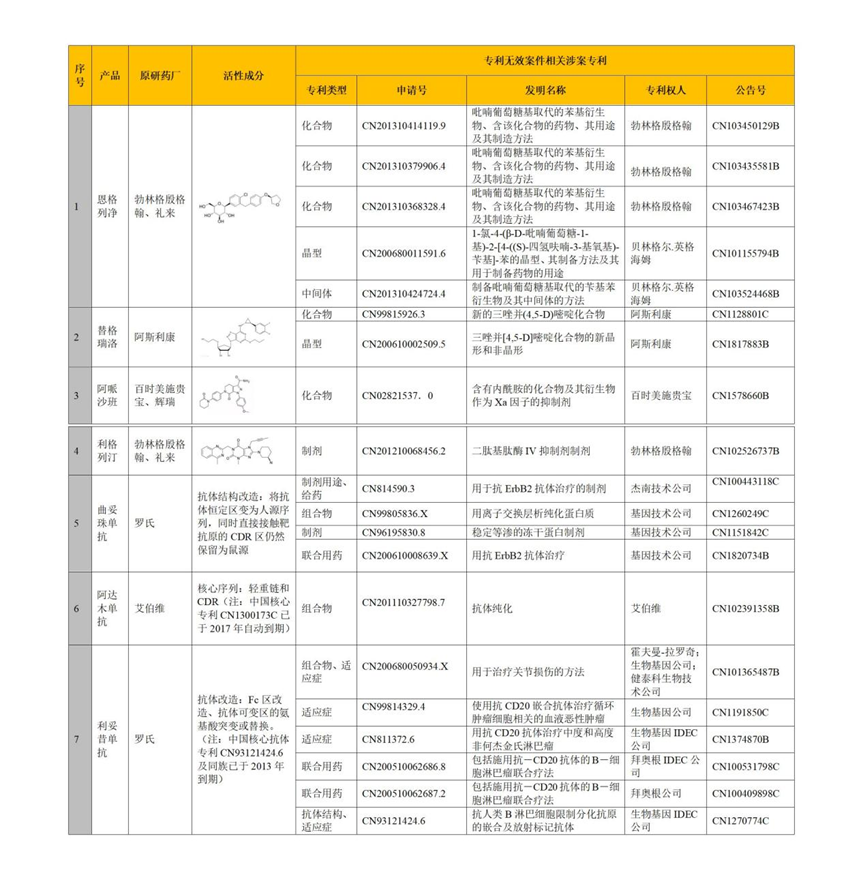
如果拟交易的药品标的对应的核心专利已授权,那么则可能需要对该等专利的稳定性进行分析,即该等专利是否存在被无效的可能性。重磅生物药、化学药被无效的案例层出不穷,而拟交易的药品尤其是涉及创新药是否构建且具备了稳定的专利保护已成为众多License-in/out 交易中的关注重点,这也就凸显了生物医药授权许可交易 License-in/out 中对拟交易标的对应的核心专利进行授权前景/稳定性分析的重要性所在。笔者总结了近年来部分重磅生物药、化学药虽然相关核心专利已授权但仍被无效挑战的案例(请见如下图 5)。其中案例 1 涉及德国勃林格殷格翰的重磅小分子化药恩格列净,作为唯一被证实可降低 2型糖尿病患者心血管死亡及全因死亡的 SGLT2 抑制剂,恩格列净 2020 年全球销售额超过38 亿美元,占据了 SGLT-2 抑制剂销量的 50%,为保护该款重磅药的核心专利,勃林格殷格翰抢先开发一系列外围专利,以形成严密的专利网战略,而笔者所在的汇业知识产权团队唐嘉伟博士即代理了德国勃林格殷格翰恩格列净系列专利201310414119.9、201310368328.4和 201310379906.4 专利无效案件,且行政诉讼维持该无效决定,获得胜诉,上述核心专利虽然已授权,但最终因我方检索到关键无效证据、说明书中并未公开任何涉及相关用途的直接效果实验以及效果实验数据、补充实验数据不被接受从而使得该等专利不具备创造性,成功使得恩格列净化合物专利被无效。
图5 重磅药物已授权专利被无效挑战典型案例
(二)拟实施区域的自由实施FTO分析(Freedom To Operate)
出于技术交易安全以及降低相关交易风险的角度考虑,一般生物医药技术交易License-in/out 中会对拟交易的目标产品在拟实施区域/授权许可区域进行自由实施 FTO (Freedom To Operate)分析。对一项技术的自由实施(Freedom to Operate 或 FTO)指的是实施人可在不侵犯他人专利权的前提下对该技术自由地进行使用和开发,并将通过该技术生产的产品投入市场。根据我国专利法第十一条规定,“发明和实用新型专利权被授予后,除本法另有规定的以外,任何单位或者个人未经专利权人许可,都不得实施其专利,即不得为生产经营目的制造、使用、许诺销售、销售、进口其专利产品,或者使用其专利方法以及使用、许诺销售、销售、进口依照该专利方法直接获得的产品。外观设计专利权被授予后,任何单位或者个人未经专利权人许可,都不得实施其专利,即不得为生产经营目的制造、许诺销售、销售、进口其外观设计专利产品”,一定程度从法律层面也说明了进行自由实施 FTO 分析的必要性。在技术交易中,我们一般会根据许可方(Licensor)提供的目标产品的技术方案展开技术层面的侵权比对,从技术层面分析拟交易的目标产品若在拟实施区域/授权许可区域内上市销售是否可能存在侵害第三方专利权的风险,通过检索、分析并对可能侵害第三方知识产权的风险进行初步判断,为交易方提出参考建议。
下面笔者将阐述下 FTO 分析的基本流程(请见如下图 6):
图6 FTO分析的基本流程
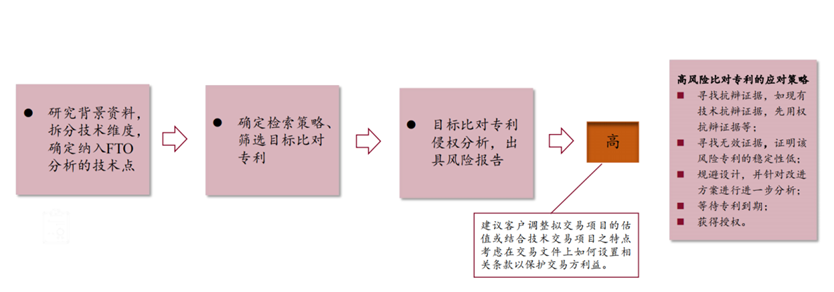
步骤1:研究背景资料,拆分技术维度,确定纳入FTO分析的技术点
在生物医药技术许可交易License-in/out 中,通过分析以及理解拟交易标的的研发背景资料、有关具体化合物结构、盐、晶型、前药、代谢物、中间体、序列、载体工具、生产工艺及制备方法、联合用药、适应症/用途等技术方案方面的临床申报材料、药监部门备案材料等,以及同行业主要竞争对手的情况,我们会拆分并归纳出拟交易标的产品的技术维度,通过与研发技术人员/客户的进一步沟通,针对风险性高低以及客户预算,最终确定纳入 FTO分析的技术点。需要说明具体的化学药、生物药在进行具体技术维度拆分时并不尽相同,同时根据具体的项目需求不同,纳入FTO分析的技术点也会有所不同。
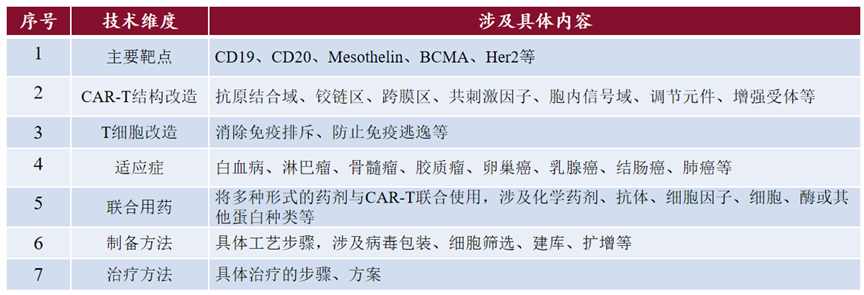
在笔者负责处理的一项关于 CAR-T 细胞治疗的 FTO 分析项目中,通过分析国内外竞品以及技术方案,归纳出了可以从主要靶点、CAR-T 结构改造、T 细胞改造、制备方法、治疗方法、适应症、联合用药等技术维度(请见如下图 7)来进行检索、分析,通过与客户商讨确定分析范围,最终初步选择了其中风险较高的几个技术点纳入 FTO 分析范围。而对于小分子化药而言,从技术维度上来看需要重点关注的是拟交易标的的活性化合物(API)是否存在侵害第三方专利的风险,如果技术交易中还涉及在拟实施区域的本地化生产,一般还可能需要考虑将原料药、制剂等生产工艺等纳入FTO分析范围,而生产工艺一般作为技术秘密进行保护,在技术交易谈判初期Licensor不一定会提供该等技术秘密细节,因此如何基于公开信息以及现有资料对此展开必要的初步核查以及分析也是生物医药技术交易 License-in/out 中需要关注的考量点之一。
图7 CAR-T细胞治疗FTO分析技术维度
步骤2:确定检索策略、筛选目标比对专利
首先基于纳入FTO分析范围的技术点确定拟交易标的产品的关键词、扩展词、IPC分类号等来构建检索式、调整检索式并进行检索,涉及小分子化药时还涉及在Reaxys数据库、STN数据库、SciFinder数据库对化合物结构进行检索,涉及大分子生物药时还涉及在数据库NCBI、Blast、STN等对序列进行检索;然后对检索结果进行专利标引、筛选目标专利以及视情况同步进行补充检索,从而最终筛选出目标比对专利。
步骤3:目标比对专利侵权分析,出具风险报告
结合专利说明书、案卷审查历史、同族专利的案卷审查情况、现有技术及公知常识等,将拟交易标的产品的技术方案与目标比对专利相应权利要求技术特征限定的的保护范围做侵权比对(Claim Chart),具体结合全面覆盖原则、等同原则以及禁反言原则等,对拟交易标的产品是否落入目标比对专利相关权利要求保护范围,即拟交易标的产品是否存在侵犯目标比对专利专利权的可能性做出判断。如果针对目标比对专利侵权可能性较低,一般应当可自由实施,如果针对目标比对专利侵权可能性较高,那么该等专利则是交易中需要重点关注的高风险专利。对于出现该等具有侵权风险的高风险专利的情况,可以建议客户结合技术交易项目的特点考虑在交易文件上设置相关条款以保护交易方利益或考虑是否调整拟交易项目的估值。同时根据交易项目需求或者临床试验以及上市申报的进度,可以进一步采取进行技术规避、寻找现有技术抗辩,以及无效该等高风险专利的证据等,如果无法规避且该等高风险专利稳定性较高,可以考虑等待专利到期或者与专利权人签订协议。
(三)拟交易产品的专利布局分析(Patent Portfolio)
另外,为了对拟交易标的产品的知识产权保护情况给出相对完备的法律意见,一般根据拟交易标的产品的技术方案以及同行业竞品的专利情况,还会调查拟交易标的是否具有完备的专利布局或者称之为专利组合。此处的专利布局组合一般涉及地域布局、或者产品技术维度布局。如果专利布局有瑕疵,根据技术交易项目处于早期、中期还是晚期,可以考虑后续是否还有相应补救完善的措施,比如递交分案申请、优先权新案申请、通过 PCT 或者巴黎公约将相关专利技术方案至少进入相应许可国家、或者申请其他的外围专利来构建更加有效的专利保护网。基于过往项目经验,交易双方还会在交易文件中设置有关专利项目团队以及全面协调和监督双方在本协议项下的专利相关的活动的条款,涉及开发和/或许可的相关专利的提交、审查、维护,也包括与许可或实施的知识产权有关的第三方专利侵权索赔以及抗辩等。
关于地域布局:在生物医药技术许可交易中,一般根据许可地域(Territory)是全球性还是区域性,即根据许可的具体国家或地区,我们在知识产权尽职调查中需要核查分析拟交易产品是否在相应的区域进行了相对完备的专利布局,而不仅仅是表面上在相应区域有专利申请而已。举例说明,比如交易许可区域涉及“大中华区(是指中国大陆、澳门、香港和台湾)以及美国”,那么在进行拟交易产品的专利布局分析时,我们就需要分析相应的专利尤其是核心专利是否已经在相应的许可国家/地区进行了相应的专利申请,比如在一项小分子化药交易中,核心专利通式化合物母案首先在中国申请,但交易许可区域除大中华区域外,还涉及美国,虽然该等核心通式化合物专利通过PCT国际专利途径进入了美国,但根据目前的审查意见(Office Action),其在美国的授权前景并不明朗,此时知识产权律师团队还需要进一步核查以及分析该等核心通式化合物专利是否在美国进行了相应的补救完善措施,比如是否进行了相应了后续申请(Continuing Application),例如分案申请 (Divisional Application)、延续申请 (Continuation Application)、或者部分延续申请(Continuation-in-part Application)等。
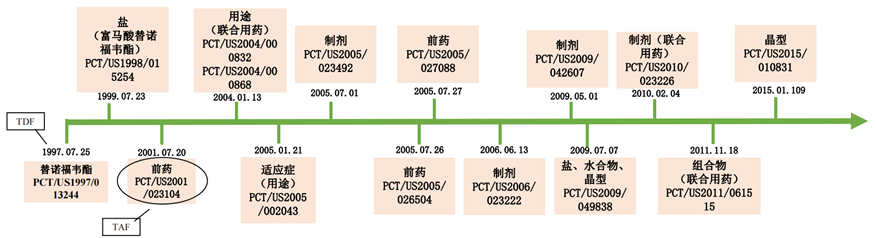
关于产品技术维度布局:生物医药的专利布局从技术维度上来看,依据不同的药品类别、具体技术方案以及研发进程的差异均会有所不同。比如笔者前述提及的 CAR-T 细胞治疗可能涉及的技术维度布局包括主要靶点、CAR-T 结构改造、T 细胞改造、制备方法、治疗方法、适应症、联合用药等。再比如小分子化药的研发历经靶点选择、先导化合物确定、活性化合物筛选、候选药物选定、制备路线优化以及药物制剂的开发等过程,这使得化药专利布局具有一定的难度和专业性,小分子化药涉及的技术维度布局通常涉及通式化合物及衍生物、药学上可接受的盐、晶型、游离酸/碱、异构体、代谢物、中间体、生产工艺及制备方法、联合用药、适应症/用途等;以示说明,笔者从化药的不同技术维度简要列举了吉利德代表性药品替诺福韦酯的部分相关专利布局,吉利德针对替诺福韦酯还布局了较多的外围专利,在此不一一进行列举(请见如下图 8)。
图 8 吉利德代表性药品替诺福韦酯相关专利技术维度布局
总体来说,拟交易标的产品是否已构建了相对完备的专利布局保护网,对于适当延长产品保护期限,以及实现专利保护价值的最大化,同样也是在生物医药技术许可交易License-in/out中进行知识产权尽职调查的关注点之一。
三、结语
从本质上来讲,生物医药技术许可交易License-in/out是一项资产交易,而许可方(Licensee)的知识产权作为交易中的重要标的,在 License-in/out 中占有非常重要的地位。在对拟交易产品进行Regular IP DD 的核查基础上,进一步从技术以及专利的角度,对拟交易的产品进行核心专利的授权前景/稳定性分析(Patentability Analyses)、拟实施区域的自由实施FTO分析(Freedom To Operate)、拟交易产品的专利布局(Patent Portfolio)分析,最终通过上述相对完备的知识产权尽职调查全面且深入的了解拟交易标的药品的相关技术实际情况,从中发现风险点以及关键问题,为交易方案的制定提供依据,并通过在交易文件中设置相应条款予以规制,保证技术交易安全以及降低交易风险。
参考:
【1】数据来源:2013-2020年数据来源于药渡咨询报告,2021年数据来源于医药魔方《2021年中国交易报告》、2022年数据来源于医药魔方《2022 年中国生物医药企业交易分析》。
【2】《专利法(2020 修订)》第二十二条:授予专利权的发明和实用新型,应当具备新颖性、创造性和实用性。
新颖性,是指该发明或者实用新型不属于现有技术;也没有任何单位或者个人就同样的发明或者实用新型在申请日以前向国务院专利行政部门提出过申请,并记载在申请日以后公布的专利申请文件或者公告的专利文件中。
创造性,是指与现有技术相比,该发明具有突出的实质性特点和显著的进步,该实用新型具有实质性特点和进步。
实用性,是指该发明或者实用新型能够制造或者使用,并且能够产生积极效果。
本法所称现有技术,是指申请日以前在国内外为公众所知的技术。







 首页
首页 上一篇
上一篇 





评论